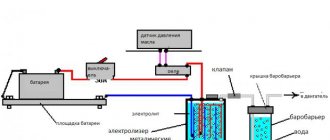
Kaedah untuk menghasilkan hidrogen dalam keadaan industri
Pengekstrakan dengan penukaran metana
... Air dalam keadaan wap, dipanaskan hingga 1000 darjah Celsius, dicampurkan dengan metana di bawah tekanan dan dengan adanya pemangkin. Kaedah ini menarik dan terbukti, perlu juga diperhatikan bahawa kaedah ini terus diperbaiki: pencarian pemangkin baru, lebih murah dan lebih berkesan, sedang dilakukan.
Pertimbangkan kaedah paling kuno untuk menghasilkan hidrogen - gasifikasi arang batu
... Sekiranya tiada akses udara dan suhu 1300 darjah Celsius, arang batu dan wap air dipanaskan. Oleh itu, hidrogen dipindahkan dari air, dan karbon dioksida diperoleh (hidrogen akan berada di puncak, karbon dioksida, juga diperoleh sebagai hasil tindak balas, berada di bahagian bawah). Ini akan menjadi pemisahan campuran gas, semuanya sangat sederhana.
Memperoleh hidrogen dengan elektrolisis air
dianggap sebagai pilihan paling mudah. Untuk pelaksanaannya, perlu menuangkan larutan soda ke dalam bekas, dan juga meletakkan dua unsur elektrik di sana. Satu akan dikenakan secara positif (anod) dan yang lain secara negatif (katod). Apabila arus digunakan, hidrogen akan menuju ke katod dan oksigen ke anod.
Memperoleh hidrogen dengan kaedah pengoksidaan separa
... Untuk ini, aloi aluminium dan galium digunakan. Ia diletakkan di dalam air, yang membawa kepada pembentukan hidrogen dan alumina semasa tindak balas. Gallium diperlukan agar tindak balas berlaku sepenuhnya (elemen ini akan mengelakkan aluminium mengoksidasi sebelum waktunya).
Perkaitan yang baru diperoleh kaedah menggunakan bioteknologi
: dalam keadaan kekurangan oksigen dan sulfur, klamidoma mula melepaskan hidrogen secara intensif. Kesan yang sangat menarik yang kini sedang dikaji secara aktif.

Jangan lupa kaedah hidrogen lama yang sudah terbukti, yang terdiri daripada penggunaan yang berbeza unsur alkali
dan air. Pada prinsipnya, teknik ini dapat dilaksanakan di persekitaran makmal dengan langkah-langkah keselamatan yang diperlukan. Oleh itu, semasa tindak balas (ia diteruskan dengan pemanasan dan dengan pemangkin), oksida logam dan hidrogen terbentuk. Tinggal hanya untuk mengumpulkannya.
Dapatkan hidrogen dengan interaksi air dan karbon monoksida
hanya mungkin dalam persekitaran industri. Karbon dioksida dan hidrogen terbentuk, prinsip pemisahannya dijelaskan di atas.

Bagaimana cara mendapatkan hidrogen dengan selamat di rumah?
Soalan-soalan seperti itu menyentuh, kerana bagi orang biasa di jalanan bahawa hidrogen cukup mudah, namun ini, walaupun dapat dilakukan dalam keadaan normal, masih berbahaya. Perkara pertama yang perlu anda ketahui ialah anda hanya perlu melakukan eksperimen sedemikian di udara terbuka (di luar), kerana hidrogen adalah gas yang sangat ringan (kira-kira 15 kali lebih ringan daripada udara biasa) dan ia akan terkumpul di dekat siling, membentuk campuran yang sangat mudah meletup. Sekiranya semua langkah yang diperlukan diambil untuk mencegah momen bermasalah, maka adalah mungkin untuk melakukan reaksi interaksi alkali dan aluminium.
Kami mengambil termos (paling baik) atau botol kaca 1/2 liter, gabus (di tengah lubang), tiub untuk mengeluarkan hidrogen, 10 gram aluminium dan vitriol (tembaga), garam meja (kira-kira 20 gram), air dalam jumlah 200 ml. dan sebiji bola (getah) untuk mengumpulkan hidrogen. Kami membeli vitriol di kedai berkebun, dan tin atau wayar bir boleh berfungsi sebagai bahan mentah aluminium. Sudah tentu, enamel dikeluarkan secara awal dengan menembak, anda memerlukan aluminium tulen, tanpa kekotoran.
Untuk 10 gram vitriol, masing-masing 100 ml air diambil, dan larutan kedua disediakan - 100 ml air akan diambil selama 20 gram garam. Warna penyelesaian adalah seperti berikut: vitriol - biru, garam - tidak berwarna. Kemudian kami mencampurkan semuanya dan kami mendapat penyelesaian kehijauan. Aluminium yang sudah siap ditambahkan kepadanya. Campuran akan mula berbuih - ini adalah hidrogen. Aluminium menggantikan tembaga dan anda dapat melihatnya dengan mata anda sendiri dengan adanya warna kemerahan pada bahan mentah aluminium. Suspensi keputihan muncul, di sinilah anda dapat mula mengumpulkan hidrogen yang kami perlukan.
Dalam prosesnya, haba tambahan diperoleh; dalam kimia, proses sedemikian disebut sebagai eksotermik. Jelas bahawa jika prosesnya tidak dikendalikan, maka sesuatu seperti geyser akan berubah, yang akan mengeluarkan sebahagian air mendidih, jadi kepekatan awal harus dikendalikan. Untuk ini, palam dengan tiub digunakan untuk membuang hidrogen ke luar dengan selamat. Diameter tiub, dengan cara itu, tidak boleh melebihi 8 milimeter dengan cara apa pun. Hidrogen yang dikumpulkan dapat digunakan untuk mengembang balon, yang akan jauh lebih ringan daripada udara di sekitarnya, yang bermaksud akan memungkinkannya naik ke atas. Sejujurnya, eksperimen sedemikian mesti dilakukan dengan sangat berhati-hati dan berhati-hati, jika tidak kecederaan dan luka bakar tidak dapat dielakkan.
INVENSI MEMPUNYAI KELEBIHAN BERIKUT
Haba yang diperoleh dari pengoksidaan gas dapat digunakan secara langsung di lokasi, dan hidrogen dan oksigen diperoleh dari pembuangan wap sisa dan air proses.
Penggunaan air yang rendah semasa menjana elektrik dan haba.
Kesederhanaan cara.
Penjimatan tenaga yang ketara sebagai ia dibelanjakan hanya untuk memanaskan pemula kepada rejim terma yang telah ditetapkan.
Produktiviti proses yang tinggi, kerana pemisahan molekul air berlangsung sepersepuluh saat.
Kaedah letupan dan keselamatan kebakaran, kerana dalam pelaksanaannya, tidak ada keperluan untuk wadah untuk mengumpulkan hidrogen dan oksigen.
Semasa operasi pemasangan, air disucikan berulang kali, diubah menjadi air suling. Ini menghilangkan enapan dan lapisan bawah, yang meningkatkan jangka hayat pemasangan.
Pemasangannya diperbuat daripada keluli biasa; kecuali dandang yang diperbuat daripada keluli tahan panas dengan lapisan dan pelindung dindingnya. Iaitu, tidak memerlukan bahan mahal khas.
Penemuan ini dapat digunakan di
industri dengan menggantikan hidrokarbon dan bahan bakar nuklear di loji janakuasa dengan air murah, meluas dan mesra alam, sambil mengekalkan kuasa loji ini.
Pandangan alternatif
Model utiliti berkaitan dengan elektrokimia dan, lebih khusus lagi, dengan tenaga hidrogen dan boleh berguna untuk mendapatkan campuran bahan bakar dengan kandungan hidrogen yang tinggi dari sebarang larutan berair.
Peranti terkenal untuk penguraian elektrokimia (pemisahan) air dan larutan akueus menjadi hidrogen dan oksigen dengan mengalirkan arus elektrik melalui air. Kelebihan utama mereka adalah kemudahan pelaksanaannya. Kelemahan utama peranti prototaip hidrogen yang diketahui ialah produktiviti rendah, penggunaan tenaga yang ketara dan kecekapan rendah. Pengiraan teoritis elektrik yang diperlukan untuk pengeluaran 1 m3 hidrogen dari air adalah 2,94 kWh, yang masih menyukarkan penggunaan kaedah hidrogen ini sebagai bahan bakar mesra alam dalam pengangkutan.
—
Peranti terdekat (prototaip) dengan reka bentuk dan tujuan yang sama dengan model utiliti yang dituntut dengan kombinasi ciri adalah elektrolisis terkenal - penjana hidrogen termudah yang mengandungi ruang berongga dengan larutan berair (air), elektrod yang diletakkan di dalamnya, dan sumber elektrik yang disambungkan kepada mereka (buku. Ensiklopedia kimia ", ayat 1, m., 1988, hlm. 401)
Intipati prototaip - penjana hidrogen yang diketahui terdiri dalam pemisahan elektrolitik air dan larutan berair di bawah tindakan arus elektrik pada H2 dan O2.
Kekurangan prototaip terdiri daripada produktiviti hidrogen rendah dan penggunaan tenaga yang ketara
Tujuan penemuan ini adalah pemodenan peranti untuk meningkatkan kecekapan tenaganya
Hasil teknikal, model utiliti ini terdiri daripada peningkatan teknikal dan tenaga peranti yang diketahui, yang diperlukan untuk mencapai tujuan ini.
Hasil teknikal yang ditentukan dicapai oleh kenyataan bahawa alat yang diketahui yang mengandungi ruang berongga dengan larutan berair, elektrod yang diletakkan di dalam air, sumber elektrik yang bersambung dengannya, dilengkapi dengan kapilari yang diletakkan secara menegak di dalam air, dengan hujung atas di atas permukaan air, dan elektrod rata, salah satunya diletakkan di bawah kapilari, dan elektrod kedua terbuat dari mesh dan terletak di atasnya, dan sumber kuasa terbuat dari voltan tinggi dan boleh laras dalam amplitud dan frekuensi, dan jurang antara hujung kapilari dan elektrod kedua dan parameter elektrik yang dibekalkan ke elektrod dipilih sesuai dengan syarat memastikan produktiviti hidrogen maksimum, dan kapasiti pengatur adalah pengatur voltan dari sumber tersebut dan pengatur jurang antara kapilari dan elektrod kedua, dan peranti ini juga dilengkapi oleh dua penjana ultrasonik, salah satunya terletak di bawah hujung bawah kapilari ini dan yang kedua - di atas hujung atasnya, dan peranti Unit ini juga dilengkapi dengan disosiator elektronik molekul kabut air yang diaktifkan yang mengandungi sepasang elektrod yang terletak di atas permukaan cecair, dengan satahnya tegak lurus dengan permukaan cecair, dan disambungkan secara elektrik ke penjana elektronik tambahan denyut frekuensi tinggi voltan tinggi dengan frekuensi dan kitaran tugas yang dapat diselaraskan, dalam julat frekuensi yang bertindih dengan frekuensi pengujaan resonan molekul sejatan cecair dan ionnya.
Video promosi:
HURAIAN PERANGKAT DALAM STATIK
Peranti untuk menghasilkan hidrogen dari air (Rajah 1) terdiri daripada bekas dielektrik 1, dengan larutan cecair 2 berair yang dituangkan ke dalamnya, dari bahan kapilari berpori halus 3, sebahagiannya direndam dalam cecair ini dan dibasahi sebelumnya. Peranti ini juga merangkumi elektrod logam voltan tinggi 4, 5 , diletakkan di hujung kapilari 3, dan disambungkan secara elektrik ke terminal sumber voltan tinggi yang diatur dari medan elektrik tanda tetap 10, dan salah satu elektrod 5 dibuat dalam bentuk plat jarum berlubang, dan diposisikan secara bergerak di atas hujung kapilari 3, sebagai contoh, selari dengannya pada jarak yang cukup untuk mengelakkan kerosakan elektrik ke sumbu yang dibasahi 3. Elektrod voltan tinggi 4 yang lain diletakkan di dalam cecair selari dengan hujung bawah kapilari, misalnya, bahan berpori 3 Peranti ini dilengkapi dengan dua penjana ultrasonik 6, salah satunya terletak di dalam cecair 2, hampir di bahagian bawah bekas 1, dan yang kedua terletak di atas paras cecair, misalnya mesh elektrod 5.
Peranti ini juga mengandungi penyekat elektronik molekul kabut air yang diaktifkan, yang terdiri daripada dua elektrod 7,8, yang terletak di atas permukaan cecair, dengan satahnya tegak lurus dengan permukaan cecair, dan disambungkan secara elektrik ke penjana elektronik tambahan 9 nadi frekuensi tinggi voltan tinggi dengan frekuensi dan kitaran tugas yang boleh diselaraskan, dalam frekuensi julat yang bertindih dengan frekuensi resonans pengujaan molekul-molekul sejat cecair dan ionnya.Peranti ini juga dilengkapi dengan loceng 12, yang terletak di atas tangki 1 - pengumpul gas pengumpulan 12, di tengahnya terdapat paip keluar untuk menarik gas bahan bakar dan H2 kepada pengguna. Pada dasarnya, unit peranti yang mengandungi elektrod 4,5 dari unit voltan tinggi 10 dan unit kapilari 3 4, 5, 6 adalah peranti gabungan pam elektroosmotik dan penyejat elektrostatik cecair 2 dari bekas 1 ... Unit 10 membolehkan anda mengatur kitaran denyut nadi dan intensiti medan elektrik berterusan dari 0 hingga 30 kV / cm. Elektrod 5 diperbuat daripada logam berlubang atau mesh untuk memberikan kemungkinan berlalunya halangan kabut air yang terbentuk dan gas bahan bakar dari hujung kapilari 3. Peranti ini mempunyai pengatur dan peranti untuk mengubah frekuensi denyutan dan amplitud mereka dan kitaran tugas, dan juga untuk mengubah jarak dan kedudukan elektrod 5 relatif terhadap permukaan penyejat kapilari 3 (mereka tidak ditunjukkan dalam Rajah 1).
HURAIAN PERANTI OPERASI PERANTI (RAJAH 1)
Pertama, larutan berair dituangkan ke dalam bekas 1, contohnya, air yang diaktifkan atau campuran bahan bakar air (emulsi) 2, penyejat 3-kapur kapilari terlebih dahulu dibasahi dengannya. Kemudian, sumber voltan tinggi 10 dihidupkan dan perbezaan potensi voltan tinggi dibekalkan ke penyejat kapilari 3 melalui elektrod 4,5, dan elektrod berlubang 5 diletakkan di atas permukaan permukaan hujung kapilari 3 pada jarak yang cukup untuk mengelakkan kerosakan elektrik antara elektrod 4,5. Akibatnya, di sepanjang serat kapilari 3 di bawah tindakan elektroosmotik dan, sebenarnya, daya elektrostatik medan elektrik membujur, gugus air sebahagiannya pecah dan disusun dalam ukuran, diserap ke kapilari 3. Lebih-lebih lagi, molekul cecair terpolarisasi dipol terungkap sepanjang vektor medan elektrik dan bergerak dari bekas ke kapilari hujung atas 3 ke potensi elektrik elektrod 5 yang bertentangan (elektroosmosis). Kemudian mereka, di bawah tindakan daya elektrostatik, terkoyak oleh daya medan elektrik ini dari permukaan permukaan hujung kapilari 3 - pada dasarnya penyejat elektroosmotik dan berubah menjadi kabus air elektrik terpolarisasi yang berpisah. Kabus air di atas elektrod 5 ini kemudian juga diperlakukan secara intensif dengan medan elektrik frekuensi tinggi berdenyut berdenyut yang dibuat di antara elektrod melintang 7,8 oleh penjana frekuensi tinggi elektronik 9. Dalam proses perlanggaran kuat molekul dan air dipol tersejat kluster di atas cecair dengan molekul udara dan ozon, elektron di zon pengionan antara elektrod 7, 8, penambahan intensif tambahan (radiolysis) kabut air diaktifkan berlaku dengan pembentukan gas yang mudah terbakar. Selanjutnya, gas bahan bakar yang diperoleh ini mengalir secara bebas ke atas ke dalam loceng pengumpul gas 12 dan kemudian melalui saluran keluar 13 dibekalkan kepada pengguna untuk menyiapkan campuran bahan bakar sintetik, misalnya, ke dalam saluran pengambilan enjin pembakaran dalaman dan memasangnya ke pembakaran ruang kenderaan bermotor. Komposisi gas yang mudah terbakar ini merangkumi molekul hidrogen (H2), oksigen (O2), wap air, kabut (H2O), serta molekul organik aktif yang disejat sebagai sebahagian daripada bahan tambahan hidrokarbon lain. Sebelum ini, kebolehoperasian peranti ini ditunjukkan secara eksperimen dan didapati bahawa intensiti proses penyejatan dan pemisahan molekul larutan berair sangat bergantung dan berubah bergantung pada parameter medan elektrik sumbernya 9,10. (Intensiti, daya), pada jarak antara elektrod 4, 5, di kawasan penyejat kapilari 3, bergantung pada jenis cecair, ukuran kapilari dan kualiti bahan kapilari 3.Pengatur yang tersedia dalam peranti ini membolehkan anda mengoptimumkan prestasi gas bahan bakar bergantung pada jenis dan parameter larutan berair dan reka bentuk khusus elektrolisis ini. Oleh kerana dalam alat ini larutan cecair berair secara intensif menguap dan berpisah sebahagiannya menjadi H2 dan O2, di bawah tindakan electroosmosis kapilari, dan ultrasound, dan kemudian secara aktif berpisah kerana pertembungan molekul sengit larutan akueus yang tersejat dengan cara medan elektrik resonan melintang tambahan, alat untuk menghasilkan hidrogen dan gas bahan api menggunakan sedikit elektrik dan oleh itu jauh lebih menjimatkan oleh puluhan ratus kali lebih ekonomik daripada penjana hidrogen elektrolisis yang diketahui.
TUNTUTAN
Peranti ultrasonik untuk menghasilkan hidrogen dari larutan berair, yang mengandungi bekas dengan larutan berair, elektrod logam yang diletakkan di dalamnya, dan sumber elektrik yang bersambung dengannya, dicirikan dalam hal ituia dilengkapi dengan kapilari yang diletakkan secara menegak di ruang ini, dengan hujung atasnya di atas paras larutan berair, dan salah satu daripada dua elektrod diletakkan di dalam cecair di bawah kapilari, dan elektrod kedua dibuat bergerak dan dilapisi grid dan diletakkan di atas mereka, dan sumber kuasa terbuat dari voltan tinggi dan boleh laras dalam amplitud dan frekuensi, dan peranti ini juga dilengkapi oleh dua penjana ultrasonik, salah satunya terletak di bawah hujung kapilari bawah ini dan yang kedua terletak di atas bahagian atasnya hujungnya, dan peranti ini juga dilengkapi dengan resonan elektronik penyekat molekul kabut air yang diaktifkan yang mengandungi sepasang elektrod yang terletak di atas permukaan cecair, dengan pesawatnya, tegak lurus dengan permukaan cecair, dan disambungkan secara elektrik ke penjana elektronik tambahan denyutan frekuensi tinggi voltan tinggi dengan frekuensi dan kitaran tugas yang boleh disesuaikan, dalam julat frekuensi yang mengandungi frekuensi pengujaan resonan molekul cecair tersejat dan ionnya.
TUNTUTAN
Kaedah untuk menghasilkan hidrogen dan oksigen dari wap air
, termasuk mengalirkan wap ini melalui medan elektrik, yang dicirikan kerana mereka menggunakan wap air yang terlalu panas dengan suhu
500 - 550 o C
, melalui medan elektrik arus terus voltan tinggi untuk memisahkan wap dan memisahkannya menjadi atom hidrogen dan oksigen.
Saya sudah lama mahu melakukan perkara yang serupa. Tetapi percubaan lebih lanjut dengan bateri dan sepasang elektrod tidak tercapai. Saya mahu membuat alat lengkap untuk penghasilan hidrogen, dalam kuantiti yang banyak untuk mengembang balon. Sebelum membuat alat lengkap untuk elektrolisis air di rumah, saya memutuskan untuk memeriksa semua yang ada pada model ini.
Skema umum elektrolisis kelihatan seperti ini.
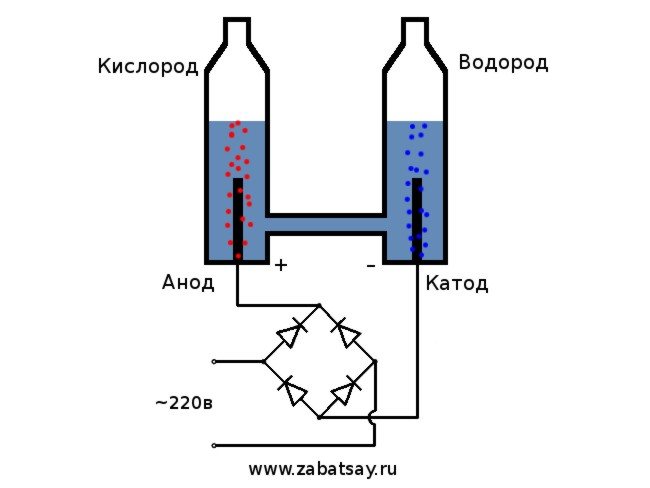

Model ini tidak sesuai untuk penggunaan seharian penuh. Tetapi kami berjaya menguji idea tersebut.
Oleh itu, saya memutuskan untuk menggunakan grafit untuk elektrod. Sumber grafit yang sangat baik untuk elektrod adalah pengumpul bas troli. Terdapat banyak dari mereka yang terbaring di penghentian akhir. Perlu diingat bahawa salah satu elektrod akan runtuh.


Kami melihat dan menyelesaikan dengan fail. Keamatan elektrolisis bergantung pada kekuatan arus dan luas elektrod.


Wayar dipasang pada elektrod. Wayar mesti dilindungi dengan teliti.


Untuk model sel elektrolitik, botol plastik cukup sesuai. Lubang dibuat di penutup untuk paip dan wayar.


Semuanya dilapisi dengan baik dengan sealant.


Leher botol yang dipotong sesuai untuk menyambungkan dua bekas.


Mereka perlu disatukan dan jahitan mesti dicairkan.


Kacang dibuat dari penutup botol.


Lubang dibuat dalam dua botol di bahagian bawah. Segala-galanya dihubungkan dan diisi dengan teliti dengan sealant.


Kami akan menggunakan rangkaian isi rumah 220V sebagai sumber voltan.Saya ingin memberi amaran kepada anda bahawa ini adalah mainan yang agak berbahaya. Oleh itu, jika anda tidak mempunyai kemahiran yang mencukupi atau terdapat keraguan, maka lebih baik tidak mengulanginya. Di rangkaian isi rumah, kita mempunyai arus bolak-balik, untuk elektrolisis mesti diluruskan. Jambatan diod sangat sesuai untuk ini. Foto dalam gambar tidak cukup kuat dan cepat habis. Pilihan terbaik adalah jambatan diod MB156 Cina dalam kotak aluminium.


Jambatan diod menjadi sangat panas. Penyejukan aktif akan diperlukan. Penyejuk untuk pemproses komputer sangat sesuai. Kotak persimpangan dengan ukuran yang sesuai boleh digunakan untuk kandang. Dijual dalam barangan elektrik.


Beberapa lapisan kadbod mesti diletakkan di bawah jambatan dioda.


Lubang yang diperlukan dibuat di penutup kotak persimpangan.


Seperti inilah unit pemasangan. Electrolyzer dikuasakan dari sumber, kipas dikuasakan oleh sumber kuasa sejagat. Larutan baking soda digunakan sebagai elektrolit. Di sini mesti diingat bahawa semakin tinggi kepekatan larutan, semakin tinggi kadar tindak balasnya. Tetapi pada masa yang sama, pemanasan juga lebih tinggi. Lebih-lebih lagi, tindak balas penguraian natrium pada katod akan menyumbang kepada pemanasan. Tindak balas ini adalah eksotermik. Hasilnya, hidrogen dan natrium hidroksida akan terbentuk.


Peranti dalam foto di atas sangat panas. Ia mesti dimatikan secara berkala dan tunggu sehingga ia sejuk. Masalah pemanasan sebahagiannya diselesaikan dengan menyejukkan elektrolit. Untuk ini saya menggunakan pam pancut meja. Tiub panjang mengalir dari satu botol ke botol yang lain melalui pam dan baldi air sejuk.


Kesesuaian masalah ini hari ini cukup tinggi kerana fakta bahawa skop penggunaan hidrogen sangat luas, dan dalam bentuk tulennya praktikalnya tidak terdapat di mana-mana alam. Itulah sebabnya beberapa teknik telah dikembangkan yang membolehkan pengekstrakan gas ini dari sebatian lain melalui tindak balas kimia dan fizikal. Perkara ini dibincangkan dalam artikel di atas.
Lelaki itu membuat pemasangan untuk menghasilkan hidrogen
Ursu Rom. Dalam video ini saya ingin menunjukkan bagaimana anda boleh membuat penjana kecil dari 10 pisau pencukur yang akan mengeluarkan hidrogen dari air. Untuk memulakan, anda memerlukan unit bekalan kuasa dari 5 hingga 12 volt, kekuatan semasa dari 0,5 hingga 2 ampere. Wayar tembaga, balang kaca dengan penutup skru tertutup. Sebotol plastik, sekeping pembaris plastik. Dua penitis. 10 bilah. Garam yang boleh dimakan. Alat: besi pematerian, pistol gam, pisau alat tulis.


Produk untuk pencipta